Centre de ressources

Quels critères orientent le choix des hygiénistes en matière de DHN afin de prévenir le risque infectieux ?
Les critères clés
L’objectif principal est la maîtrise du risque infectieux, afin de protéger à la fois les patients et le personnel soignant. La désinfection des dispositifs invasifs semi-critiques, tels que les endoscopes ou les sondes endocavitaires, est une étape cruciale pour prévenir la transmission de pathogènes responsables des infections associées aux soins (IAS).
Le choix d’un équipement de désinfection ne peut donc pas être laissé au hasard : il repose sur des critères rigoureux et bien définis.
1. La conformité réglementaire
Chaque année, 4,3 millions de cas d’infections associées aux soins IAS sont recensées en Europe1. Une part non négligeable est liée à la contamination de dispositifs médicaux insuffisamment désinfectés, comme les sondes endocavitaires. Ces infections peuvent entraîner des complications sévères, causées notamment par des pathogènes tels que le Staphylococcus aureus, les entérocoques, ou encore le HPV.
Chez certains patients, ces infections peuvent évoluer vers des formes invasives voire mortelles. En conséquence, un cadre réglementaire strict encadre les dispositifs de désinfection. Les recommandations du ministère de la Santé et de la SF2H regroupées dans Guide de bonnes pratiques de traitement des dispositifs médicaux réutilisables (2022) sont à cet égard très claires.
Il est ainsi recommandé :
- de réaliser systématiquement une désinfection de niveau intermédiaire entre chaque patient pour les sondes endocavitaires
- d’utiliser une protection adaptée (type gaine) pour chaque examen
Ces dispositifs sont classés comme "semi-critiques" selon la classification de Spaulding, en raison de leur contact potentiel avec la peau non intacte, les muqueuses ou le sang.
Le dispositif de désinfection utilisé doit donc obligatoirement être classé IIb.
Mais pourquoi la classe IIb ?
Les automates de désinfection sont considérés comme des dispositifs médicaux actifs. À ce titre, les règles de classification 9 à 13 du Règlement (UE) 2017/745 (MDR) s’appliquent. Mais surtout, c’est la règle 16 (Annexe VIII) qui est déterminante : celle-ci s’applique aux dispositifs destinés à désinfecter des dispositifs médicaux invasifs.
- Les dispositifs de classe IIa ne couvrent que la désinfection de dispositifs non invasifs.
- En revanche, la classe IIb est exigée pour les dispositifs utilisés sur des dispositifs médicaux invasifs comme les sondes endovaginales ou autres endoscopes.
Pour revendiquer une Désinfection de Haut Niveau (DHN), il faut également des preuves de performance robustes.
2. L'efficacité du dispositif de désinfection
La norme NF EN 14885:2022 permet d’évaluer l’efficacité des dispositifs et produits désinfectants. Elle définit les standards requis pour une activité : bactéricide, levuricide & fongicide, mycobactéricide, virucide et sporicide.
Ces critères sont adaptés aux exigences de la médecine humaine. Le tableau ci-dessous regroupe les référentiels normatifs auxquels un dispositif de désinfection doit répondre pour être considéré comme sûr et efficace. Les micro-organismes testés sont ceux couramment responsables des IAS. L’efficacité est évaluée par la réduction logarithmique des souches après un cycle de Désinfection de Haut Niveau.
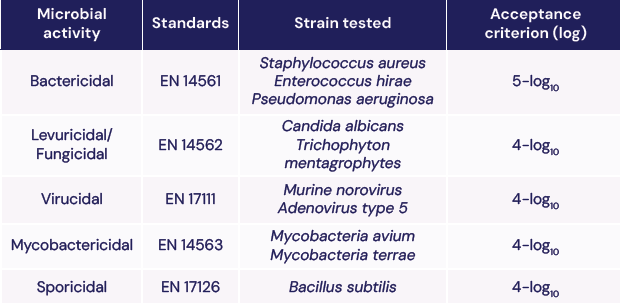
Par exemple :
- Enterococcus hirae et Staphylococcus aureus, impliqués dans les endocardites infectieuses, doivent être efficacement éliminés.
3. La traçabilité
La traçabilité est un élément clé de la gestion du risque d'infection. Il est essentiel de pouvoir identifier quel dispositif a été désinfecté, par qui, et à quel moment, afin de :
- limiter les risques de contamination croisée,
- et de réagir rapidement en cas d’incident ou de suspicion de chaîne de contamination.
Cette étape indispensable, doit être réalisée avec rigueur tout en restant peu chronophage pour le personnel
La SF2H rappelle, dans son Guide de bonnes pratiques de traitement des dispositifs médicaux réutilisables (2022) , que la traçabilité des procédures de désinfection est obligatoire : il doit être possible de retrouver, pour chaque patient, le matériel utilisé et les conditions de désinfection associées.
Le ministère de la Santé va plus loin dans l’INSTRUCTION N° DGOS/PF2/DGS/VSS1/2016/220 du 4 juillet 2016 relative à relative au traitement des endoscopes souples thermosensibles à canaux au sein des lieux de soins en préconisant une traçabilité croisée entre : le patient, la sonde (ou le dispositif utilisé), et le cycle de désinfection effectué
Une traçabilité manuelle est acceptée, mais une traçabilité informatisée est fortement recommandée, notamment pour permettre un accès aux données en dehors des heures ouvrées et garantir une exhaustivité et une sécurisation optimales des informationsii.
4. L'avis des utilisateurs
Pour que les pratiques évoluent vers une désinfection toujours plus efficace, il est indispensable de prendre en compte la réalité du terrain. Impliquer les professionnels de santé, en particulier les utilisateurs finaux, est une condition essentielle pour garantir l’acceptation et l’appropriation du changement.
La mise en place d’essais sur une période définie permet de recueillir des retours concrets et objectifs. Ces essais sont essentiels pour évaluer plusieurs critères déterminants :
- Réponse aux besoins spécifiques de l’établissement ou du service concerné,
- Optimisation du flux de travail : gain de temps, simplicité d’utilisation, meilleure maîtrise du risque infectieux,
- Prise en main intuitive du dispositif et formation rapide des utilisateurs,
- Amélioration de la Qualité de Vie au Travail (QVT) : réduction de l’exposition aux produits chimiques, diminution du stress lié aux manipulations, baisse du risque d’erreurs humaines.
Ces retours d’expérience permettent de guider le choix final vers une solution non seulement performante sur le plan microbiologique, mais aussi adaptée aux pratiques et contraintes du quotidien hospitalier.
Pourquoi le Chronos® Max répond à toutes les exigences ?
Faire le bon choix en matière de désinfection est essentiel pour une hygiéniste. Le Chronos® Max de Germitec s’impose comme une solution fiable, conforme et performante pour assurer une Désinfection de Haut Niveau des dispositifs médicaux invasifs, tout en répondant aux attentes réglementaires et opérationnelles du terrain.
✅ Conformité réglementaire
- Classé dispositif médical de classe IIb, le Chronos® Max est marqué CE, en conformité avec le règlement européen MDR 2017/745.
- Il est conçu pour la DHN des sondes endocavitaires, garantissant un haut niveau de sécurité pour les patients et le personnel de santé.
✅ Efficacité validée
Les tests réalisés par Eurofins Biotech-Germande, laboratoire indépendant, démontrent une conformité à la norme NF EN 14885:2022, avec une efficacité prouvée contre :
- Enterococcus hirae et Staphylococcus aureus, agents fréquents des IAS,
- le HPV, notamment les souches 16 et 18, reconnues pour leur potentiel oncogène élevé.
Traçabilité fiable et intégrée
Le Chronos® Max propose une traçabilité complète et simple à mettre en œuvre :
- Détection automatique de la sonde dans la chambre de désinfection (technologie brevetée),
- Traçabilité papier via imprimante intégrée,
- Traçabilité numérique avec le logiciel Germitrac®, pour un accès rapide à l’historique des cycles, même hors horaires ouvrés.
✅ Une solution pensée pour les utilisateurs
Sans produits chimiques, le Chronos® Max offre une désinfection rapide et sûre, tout en allégeant la charge des équipes :
- Cycle court et automatisé,
- Interface intuitive,
- Gain de temps, sécurité et confort au quotidien.
En savoir plus sur Chronos® Maxnotre appareil de désinfection UV-C de haut niveau pour les services de cardiologie et d'ORL.
--------
* Produit disponible en Europe et en Océanie, non disponible aux États-Unis.
Références :
1. Source : Enquête de prévalence ponctuelle de l'ECDC (2016-2017)
2. Instruction n° DGOS/PF2/DGS/VSS1/2016/220 du 4 juillet 2016





